MILENIO
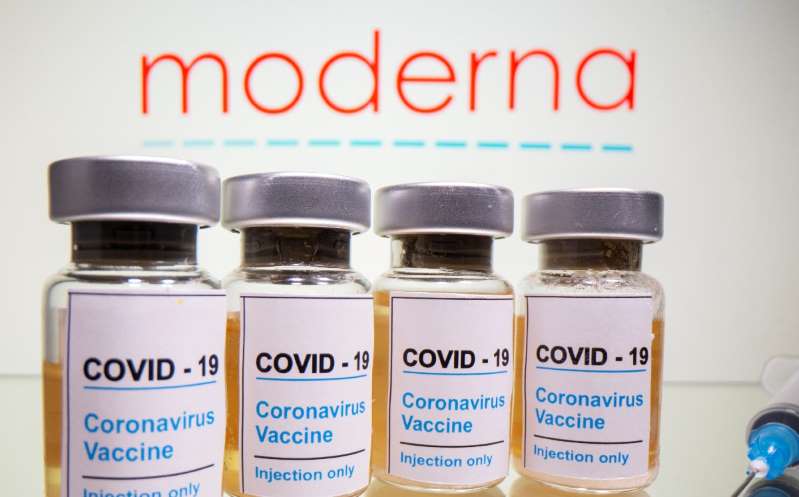
Moderna Inc dijo que solicitará la autorización de uso de emergencia en Estados Unidos y la Unión Europea de su vacuna contra el covid-19, basada en los resultados completos de la última etapa de un estudio que mostró que su vacuna tiene una efectividad del 94,1%, sin preocupaciones serias de seguridad.
Asimismo, reportó un éxito del 100% en la prevención de casos graves. La solicitud convertirá posiblemente el producto de Moderna en la segunda vacuna que recibirá autorización de uso de emergencia este año.
“Creemos que tenemos una vacuna con una gran eficacia. Ahora tenemos los datos que lo demuestran.Esperamos jugar un papel importante en la derrota de esta pandemia”, dijo Ral Zaks, presidente médico de la firma, en una entrevista telefónica.
BREAKING: Moderna's coronavirus vaccine shows efficacy of 100% against severe coronavirus infections
— The Spectator Index (@spectatorindex) November 30, 2020
Zaks dijo que se emocionó al ver el resultado del 94,1% durante el fin de semana:
“Es la primera vez que me permití llorar. Con este nivel de efectividad, cuando uno hace las cuentas de lo que esto significa para la pandemia que nos rodea, es simplemente apabullante”.
Según la compañía, el análisis de eficacia del estudio de fase 3 de la vacuna de Moderna incluyó a 30 mil participantes con una eficacia del 94.1%, con una tolerancia generalmente buena y sin que se hayan identificado problemas de seguridad graves hasta la fecha.
El estudio de la fase 3 ha superado los 2 meses de seguimiento medio después de la vacunación, según lo exige la FDA de Estados Unidos para la autorización de uso de emergencia, dice la compañía en un comunicado.
You may also like
-
En beneficio de las niñez con cáncer, ONS anuncian el “National Pancake Day”
-
Encuentran cadáver en la carretera federal Tehuacán-Orizaba
-
Se ahogaron dos personas en laguna de Chignahuapan
-
Mujer muerta y dos personas con crisis nerviosa en diferentes accidentes
-
Mujer falleció tras accidente en carretera Puebla-Tlaxcala