ABC NOTICIAS
Se trata del primer medicamento autorizado a nivel de la Unión Europea para el tratamiento de la Covid-19
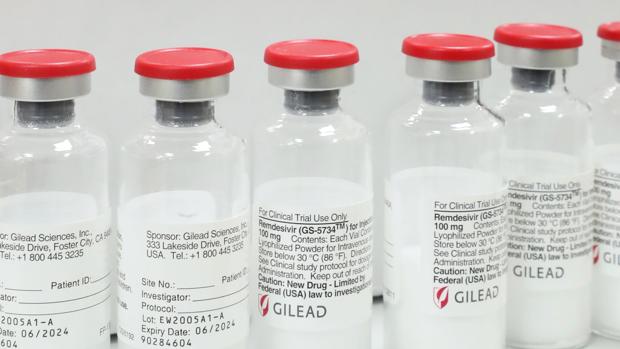
La Comisión Europea ha autorizado este viernes la comercialización condicional en el bloque del Remdesivir, el antiviral para tratar la COVID-19, apenas una semana después de que la Agencia Europea del Medicamento (EMA) recomendara su uso, según ha informado en un comunicado.
Según Bruselas, el permiso se ha conseguido en un plazo «excepcionalmente corto» gracias procedimiento acelerado que ha contado con el visto bueno también de los Estados miembros y que ha permitido acortar los tiempos frente a los 67 días de media que se suele tardar en conceder estas autorizaciones, indica EP.
Las autorizaciones condicionales son otorgadas a aquellos fármacos en los que los beneficios derivados de su uso compensan el riesgo derivado de que haya menos datos de los que normalmente se exigen para las autorizaciones completas, según explica la EMA en su página web.
La comisaria de Salud y Seguridad Alimentaria, Stella Kyriakides, ha destacado que esta autorización preliminar concedida al Remdesivir es «un importante paso adelante en la lucha contra el virus». También ha asegurado que el hecho de que se haya otorgado «menos de un mes después de la solicitud muestra claramente la determinación de la UE para responder rápido cuando haya nuevos medicamentos disponibles».
«No escatimaremos en esfuerzos para garantizar tratamientos eficientes o una vacuna contra el coronavirus», ha subrayado la comisaria chipriota en un comunicado.
Acuerdos con la farmacéutica
El anuncio llega, además, un día después de que el Ejecutivo comunitario confirmara que está negociando con Gilead Sciences la reserva de viales de este antiviral, un movimiento que se ha conocido después de que Estados Unidos anunciase un acuerdo con la farmacéutica para asegurarse el suministro de este fármaco hasta septiembre.
«La Comisión también está actualmente en negociaciones con Gilead sobre la posibilidad de reservar dosis de Remdesivir para los Estados miembros», expresó este jueves en una rueda de prensa el portavoz de Salud del Ejecutivo comunitario, Stefan De Keersmaecker.
Ante la compra masiva estadounidense, la directora de la Agencia Española del Medicamento (AEM), María Jesús Lamas, ha asegurado que España cuenta con un reservas suficiente de Remdesivir. Ha dicho que la comunicación con la compañía que produce el fármaco, Gilead, es «continua» y que ha confirmado que las compras pactadas anteriormente se mantienen vigentes.
Lamas ha explicado que en España el Remdesivir se está usando desde febrero contra el Covid-19 y que, además, se ha llevado a cabo un «seguimiento estricto». «Le hemos pedido a la filial española que traiga el máximo número de dosis posible. Pero el ‘stock’ será suficiente hasta que se incremente su producción, en otoño. Dada la situación epidemiológica, el ”stock’ de Remdesivir que hay en España es suficiente. No nos podemos plantear la situación si se repite lo de marzo o abril, pero eso no es esperable».
You may also like
-
Motociclistas, el sector más numeroso de fallecidos por accidentes viales en Puebla capital este año
-
Venezuela deporta a Estados Unidos a Alex Saab, operador financiero clave de Maduro
-
Murió empleado en la caseta Cuacnopalan-Oaxaca
-
Acumula Puebla 225 positivos de sarampión
-
Israel mata al líder del brazo armado de Hamás