PRNewswire
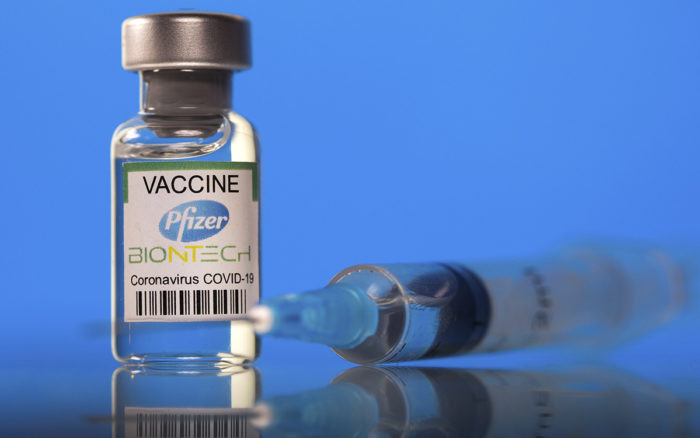
La Agencia Nacional de Vigilancia Sanitaria (Anvisa) recibió de la farmacéutica Pfizer el pedido de autorización para el uso de emergencia de una segunda vacuna contra el covid-19. La nueva vacuna es del tipo bivalente, es decir, actúa contra dos cepas del virus. En este caso, consiste en una mezcla de la cepa original, utilizada en la vacuna ComiRNAty, ya aplicada en Brasil desde febrero de 2021, y la cepa Ómicron, subvariante BA.1.
Una vez recibida la solicitud de autorización para uso de emergencia, Anvisa tiene 30 días para completar la evaluación. Este plazo se interrumpe siempre que sea necesario solicitar a la empresa información adicional o aclaraciones sobre los datos de calidad, eficacia y seguridad presentados.
El Reino Unido fue el primer país en aprobar una vacuna destinada a combatir a la variante Ómicron. La vacuna bivalente, fabricada por el laboratorio estadounidense Moderna, tuvo su aprobación confirmada esta semana en aquel país. La decisión del organismo regulador británico se basó en ensayos clínicos que mostraron una “fuerte respuesta inmune” contra la Ómicron provocada por el inmunizador.
You may also like
-
Roku lanza Howdy en México, un servicio de suscripción de video sin anuncios
-
Artemis II concluyó su misión alrededor de la Luna y comienza su regreso
-
Los astronautas de Artemis II se convierten en los humanos que más lejos han viajado en el espacio: los 40 minutos críticos en los que perdieron contacto con la Tierra
-
Eventos astronómicos del mes de abril 2026
-
Artemis II también tiene participación hispana, ¿quiénes son los latinos clave en la misión a la Luna?